MODELOS ATÓMICOS
MODELOS ATÓMICO DE DALTON
Dalton explicó su teoría formulando una serie de enunciados simples:
- La materia está formada por partículas muy pequeñas llamadasátomos, que son indivisibles y no se pueden destruir.
- Los átomos de un mismo elemento son iguales entre sí, tienen su propio peso y cualidades propias. Los átomos de los diferentes elementos tienen pesos diferentes.
- Los átomos de elementos diferentes se pueden combinar en proporciones distintas y formar más de un compuesto.
- Los compuestos químicos se forman al unirse átomos de dos o más elementos distintos.

MODELO ATÓMICO DE THOMSON
El modelo atómico de Thomson, es una teoría sobre la estructuraatómica propuesta en 1904 por Joseph John Thomson, descubridor delelectrón[1] en 1897, mucho antes del descubrimiento del protón y delneutrón. En dicho modelo, el átomo está compuesto por electrones de carga negativa en un átomo positivo, como un pudin de pasas. Se pensaba que los electrones se distribuían uniformemente alrededor del átomo. En otras ocasiones, en lugar de una sopa de carga positiva se postulaba con una nube de carga positiva. En 1906 Thomson recibió elpremio Nobel de Física por sus investigaciones en la conducción eléctrica en gases.El átomo no deja de ser un sistema material que contiene una cierta cantidad de energía externa. Ésta provoca un cierto grado de atracción de los electrones contenidos en la estructura atómica. Desde este punto de vista, puede interpretarse que el modelo atómico de Thomson es un modelo actual como consecuencia de la elasticidad de los electrones en el coseno de la citada estructura.
MODELOS ATÓMICO DE RUTHERFORD
El modelo atómico de Rutherford es un modelo atómico o teoría sobre la estructura interna del átomo propuesto por el químico y físico británico-neozelandés Ernest Rutherford para explicar los resultados de su "experimento de la lámina de oro", realizado en 1911.
La importancia del modelo de Rutherford no residió en proponer la existencia de un núcleo en el átomo. Término que, paradójicamente, no aparece en sus escritos. Lo que Rutherford consideró esencial, para explicar los resultados experimentales, fue "una concentración de carga" en el centro del átomo, ya que si no, no podía explicarse que algunas partículas fueran rebotadas en dirección casi opuesta a la incidente. Este fue un paso crucial en la comprensión de la materia, ya implicaba la existencia de un núcleo atómico donde se concentraba toda la carga positiva y más del 99,9% de la masa. Las estimaciones del núcleo revelaban que el átomo en su mayor parte estaba vacío.
MODELO ATÓMICO DE BOHR
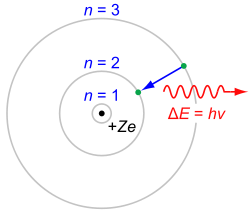
En este modelo los electrones giran en órbitas circulares alrededor del núcleo, ocupando la órbita de menor energía posible, o la órbita más cercana posible al núcleo. El electromagnetismo clásico predecía que una partícula cargada moviéndose de forma circular emitiría energía por lo que los electrones deberían colapsar sobre el núcleo en breves instantes de tiempo. Para superar este problema Bohr supuso que los electrones solamente se podían mover en órbitas específicas, cada una de las cuales caracterizada por su nivel energético. Cada órbita puede entonces identificarse mediante un número entero n que toma valores desde 1 en adelante. Este número "n" recibe el nombre de Número Cuántico Principal.
EL ÁTOMO
En química y física, átomo (del latín atomum, y éste del griego ἄτομον, sin partes)[1] es la unidad más pequeña de un elemento químico que mantiene su identidad o sus propiedades y que no es posible dividir mediante procesosquímicos.
El concepto de átomo como bloque básico e indivisible que compone la materiadel universo fue postulado por la escuela atomista en la Antigua Grecia. Sin embargo, su existencia no quedó demostrada hasta el siglo XIX. Con el desarrollo de la física nuclear en el siglo XX se comprobó que el átomo puede subdividirse en partículas más pequeñas
El núcleo del átomo se encuentra formado por nucleones, los cuales pueden ser de dos clases:
- Protones: Partícula de carga eléctrica positiva igual a una carga elemental, y 1,67262 × 10–27 kg y una masa 1837 veces mayor que la del electrón.
- Neutrones: Partículas carentes de carga eléctrica y una masa un poco mayor que la del protón (1,67493 × 10–27 kg).
El núcleo más sencillo es el del hidrógeno, formado únicamente por un protón. El núcleo del siguiente elemento en la tabla periódica, el helio, se encuentra formado por dos protones y dos neutrones. La cantidad de protones contenidas en el núcleo del átomo se conoce como número atómico, el cual se representa por la letra Z y se escribe en la parte inferior izquierda del símbolo químico. Es el que distingue a un elemento químico de otro. Según lo descrito anteriormente, el número atómico del hidrógeno es 1 (1H), y el del helio, 2 (2He).






0 comentarios:
Publicar un comentario